近日,一项由国内蚌埠医科大学学生姚凯、孙韵、田珂、张硕等本科生在导师任丽的带领下完成了一项具有重要医学价值的研究,为结直肠疾病的诊疗开辟了新的路径。该研究团队利用单细胞多组学技术,首次揭秘了结直肠疾病微环境里糖酵解重编程与程序性死亡(PCD)两大通路的交互作用,并据此建立了精准预后模型,为患者的个体化治疗提供了关键依据。

实验室平台依托
结直肠疾病是全球范围内较为常见的疾病之一,其治疗效果不佳的主要原因之一在于细胞代谢异常与免疫逃逸现象。研究人员对23例患者的65,362个单细胞进行测序分析,发现肿瘤上皮细胞中有8种糖酵解相关亚群,其中P4HA1+亚群的糖酵解活性最高,其高表达基因(如DHRS7、BOK)会显著缩短患者的生存时间。“糖酵解除了为肿瘤提供能量外,还会通过乳酸分泌改变免疫微环境,从而形成‘代谢-免疫’双重挑战。”研究负责人姚凯解释道,“我们发现P4HA1+上皮细胞亚群对患者预后影响显著,可能导致化疗耐药。”
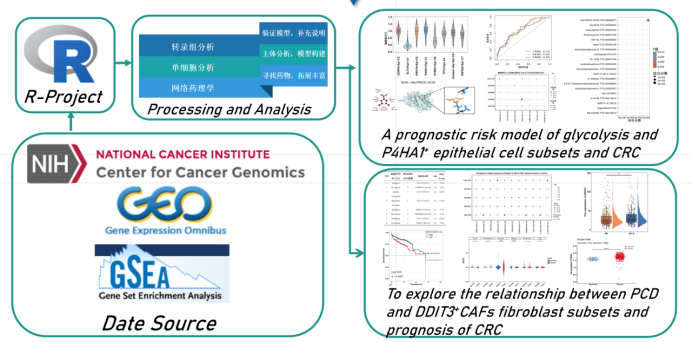
项目研究内容
基于糖酵解亚群的特征基因,研究团队通过LASSO-Cox回归分析,筛选出6个关键预后基因(DHRS7、BOK、PFN2等),构建了结直肠疾病糖酵解风险评分模型,并在多个国际队列中得到验证。该模型突破了传统分期的局限,能够更精准地识别高风险患者群体。结合临床数据构建的列线图进一步提升了实用性,目前已在多家三甲医院开展前瞻性试验。
在药物筛选过程中,研究人员发现抗癫痫药物丙戊酸能够特异性抑制P4HA1+亚群的代谢活性。体外实验显示,丙戊酸可使肿瘤细胞凋亡率提高76%。“丙戊酸的安全性已在临床得到长期验证,这一发现为老药新用提供了重要依据。”项目指导老师任丽表示,“目前团队正在进行小鼠移植瘤模型的剂量优化研究。”
研究还首次发现,副凋亡介导的DDIT3+癌症相关成纤维细胞(CAFs)通过分泌IL-6和TGF-β重塑免疫微环境,其高表达与结直肠疾病的淋巴结转移和分期显著相关。
“这类细胞就像疾病的‘免疫盾牌’,既能抑制免疫细胞的杀伤作用,又促进血管生成。”病理科张教授强调,“靶向DDIT3通路有望逆转免疫抑制状态,为免疫疗法提供新靶点。”
研究团队所建立的“代谢-死亡”双维度评估体系,为结直肠疾病的精准分类提供了新的思路。“精准诊疗的核心在于为每位患者制定最适合的策略。”项目首席科学家刘德培院士展望,“未来我们将整合更多技术手段,打造实时动态监测系统,助力实现疾病的全程管理。”
(本文图片由研究团队提供,数据来源于相关数据库)
 【广告】免责声明:本内容为广告,相关素材由广告主提供,广告主对本广告内容的真实性负责。蚌埠新闻网登载此文出于传递更多信息之目的,并不意味着赞同其观点或证实其描述。文章内容仅供参考,不构成投资、消费建议。据此操作,风险自担!!!
【广告】免责声明:本内容为广告,相关素材由广告主提供,广告主对本广告内容的真实性负责。蚌埠新闻网登载此文出于传递更多信息之目的,并不意味着赞同其观点或证实其描述。文章内容仅供参考,不构成投资、消费建议。据此操作,风险自担!!!